I) Introduction
Le cancer de prostate est le cancer le plus fréquent de la population masculine (incidence de 214 cas pour 1000) et la seconde cause de mortalité après le cancer bronchique. Si la plupart de ces cancers évolue lentement certaines formes restent agressives. Il constitue un défi pour la communauté médicale et urologique, en particulier sur les questions du dépistage et de la prise en charge thérapeutique.
II) Quel sont les facteurs de risque du cancer prostatique ?
Ce cancer touche plus fréquemment l’homme âgé. Deux tiers des hommes qui décèdent d’un cancer de prostate ont plus de 75 ans. Il est plus fréquent en Amérique du Nord et en Europe que dans les pays en voie de développement. L’origine ethnique est importante avec un facteur de risque plus élevé chez les hommes d’origine africaine, afro-américaine ou antillaise par rapport aux caucasiens. A l’inverse, le risque est moins important chez les asiatiques. Si un parent de premier degré a un cancer le risque de cancer double. Si deux parents de premier degré ou plus sont atteints le risque est multiplié par 5 à 10 fois. Le régime alimentaire peut aussi influencer le développement de la maladie. La viande rouge et les graisses insaturées semblent augmenter le risque alors que la vitamine E, le sélénium et les lycopènes (antioxydants présents dans la tomate) ont un effet protecteur. L’activité sexuelle, l’exposition aux UV et la consommation d’alcool ont été étudiées sans montrer de résultat. Des études complémentaires sont en cours. La mutation du gène BRCA (aussi impliqué dans des cancers familiaux gynécologiques) est un facteur de risque important de développer un cancer de prostate.
III) Faut-il faire un dépistage du cancer de la prostate?
Le but du dépistage est de réduire la mortalité par cancer prostatique et non pas de dépister un plus grand nombre de cancer. Les méthodes de dépistage sont basées sur le toucher rectal et le PSA. Le toucher rectal ne peut pas être utilisé isolément pour un diagnostic précoce. L’échographie endo-rectale n’a plus d’intérêt dans le dépistage. En 2009, deux grandes études prospectives randomisées sur le dépistage du cancer prostatique ont été publiées. Une étude américaine et une étude européenne . L’étude américaine PLCO (1) a inclus 76693 hommes qui ont bénéficié d’un dépistage annuel avec PSA et toucher rectal. Les investigateurs ont conclu que la mortalité spécifique du cancer de la prostate est faible et que le dépistage ne diminue pas la mortalité par cancer. Cependant 50 % des patients du bras témoin qui ne devaient pas avoir de dépistage ont eu un dosage PSA et/ou toucher rectal en dehors de l’étude. Il est donc difficile d’être formel quant aux conclusions de cette étude. L’étude européenne ERSPC (2) a inclus 162243 hommes provenant de sept pays. Le dépistage reposait sur un dosage du PSA tous les 4 ans. Les investigateurs ont conclu à une réduction de la mortalité par cancer de 20 %. Ils ont souligné cependant que le dépistage est associé à un risque de sur diagnostic puisqu’il fallait dépister 1410 patients pour diagnostiquer 48 cancers et éviter un décès par cancer. Une mise à jour du bras suédois de l’étude européenne (Göteborg) qui inclue 20000 hommes montre à 14 ans une réduction de la mortalité par cancer de prostate de 50 %. Il a fallu cette fois que 293 patients soient dépistés pour diagnostiquer 12 cancers et que 1 décès soit évité. Il est probable que l’étude américaine PLCO, de par ses biais de réalisation, ne permette pas de répondre à l’utilité ou non du dépistage. Il est cependant possible que l’étude européenne montre sur un suivi plus long une réduction de mortalité tout en diminuant le nombre de patients à dépister pour qu’un décès soit évité.
Basé sur ces deux grandes études, aucun programme de dépistage de masse n’est actuellement recommandé en France. L’Association Française d’Urologie propose un dépistage individuel et ciblé en accord avec le patient qui est informé des risques et des bénéfices. Ce dépistage sera adapté aux facteurs de risque (âge, ethnie, PSA précoce). Les recommandations classiques sont de faire un dosage annuel de PSA à partir de 50 ans et à partir de 45 ans chez les sujets à risque. Actuellement, il est proposé de faire un premier dosage du PSA à 40 ans, si le PSA est inférieur ou égal à 1 ng/ml, le prochain dosage ne sera réalisé qu’après 8 ans car le risque de développer un cancer est alors minime. Il n’est actuellement pas recommandé de faire un dosage du PSA chez les patients de plus de 75 ans car le diagnostic précoce de cancer de prostate n’a pas d’impact clinique à cet âge.
IV) DIAGNOSTIC
Stade localisé : Grâce en particulier à l’amélioration du dépistage par le dosage du PSA, le cancer de prostate est dans la majorité des cas vu à un stade localisé où il reste latent. Les troubles mictionnels comme la faiblesse du jet, les mictions trop fréquentes ou impérieuse ne sont pas un facteur de risque du cancer mais plutôt des symptômes en rapport avec l’hypertrophie bénigne de la prostate (ou adénome).
Stade localement avancé : Le malade peut être symptomatique et présenter une hématurie (sang dans les urines), une dysurie (difficulté à uriner), une hémospermie (sang dans le sperme), des douleurs du périnée ou du bas ventre. Une obstruction des reins peut entrainer des douleurs lombaires et dans les formes évoluées une insuffisance rénale.
Stade métastatique : Douleurs osseuses, perte de poids et fatigue.
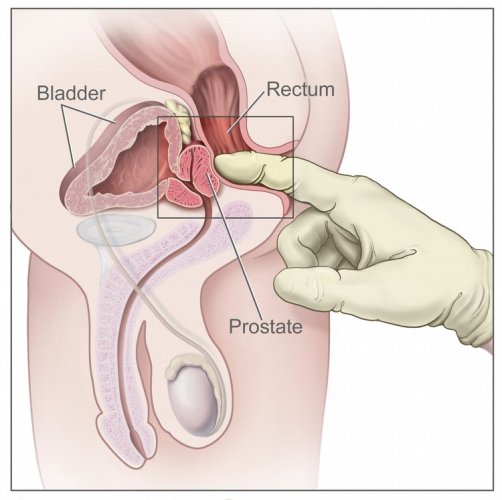
1. LE TOUCHER RECTAL
Toute anomalie du toucher rectal, asymétrie glandulaire, nodule, induration doit faire évoquer la possibilité d’un cancer de la prostate et indiquer la réalisation de biopsies écho-guidées, même si le taux de PSA est normal (standard). Chez environ 18 % des patients, le cancer est dépisté par le toucher rectal seul (3).
2. LE DOSAGE DU PSA
Le PSA ou « Prostate specific antigen » est une protéine caractéristique des cellules prostatiques dont le rôle est de fluidifier le sperme. L’augmentation de son taux traduit une anomalie prostatique qui peut être bénigne ou maligne. Bien qu’il ne soit pas spécifique du cancer, il est souvent utilisé comme marqueur tumoral. Le dosage du PSA total (valeur seuil à 4 μg/L) reste le test biologique de référence pour le dépistage et l’indication de biopsies. Les dosages répétés doivent être réalisés dans le même laboratoire et selon la même technique. Pour une valeur seuil de 4 ng/ml :
- Sensibilité (la probabilité que le test soit positif si la maladie est présente, se mesure chez les malades seulement) 75 %
- Spécificité (la probabilité d’obtenir un test négatif chez les non-malades. Elle se mesure chez les non-malades seulement) 90 %
- Valeur prédictive positive (probabilité que la maladie soit présente quand le test est positif) 30 %
- Valeur prédictive négative (probabilité que la maladie soit absente quand le test est négatif) 90 %
Un abaissement de la valeur seuil de normalité du PSA total pour un âge inférieur à 65 ans ou les groupes à risque (entre 2 et 4 μg/L) peut être proposé. Le rapport PSA libre/PSA total est utilisé chez les patients qui ont un taux de PSA situé entre 4 et 10 ng/ml pour faire la distinction entre l’adénome bénin et le cancer de prostate. Le risque de cancer à la biopsie est de 56 % quand le PSAL/T < 0,1 et de 8 % quand il est supérieur à 0,25 (4). D’autres tests de dépistage utilisant le PSA peuvent être employés comme la vélocité du PSA et la densité du PSA.
3. ECHOGRAPHIE ENDORECTALE
Cet examen largement utilisé a en fait peu d’utilité dans le diagnostic et le dépistage du cancer prostatique.
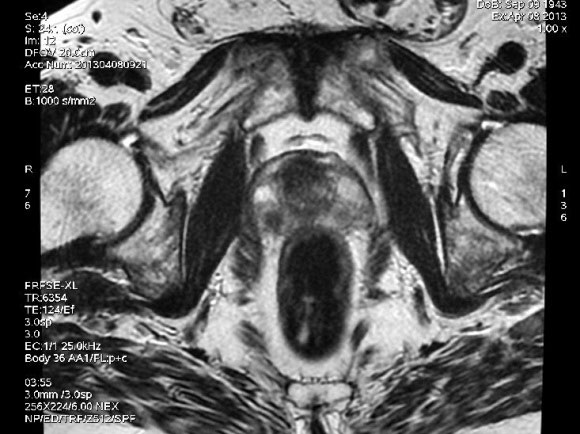
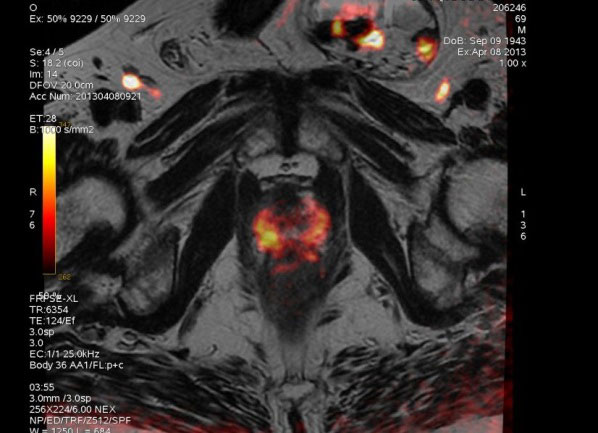
4. IMAGERIE PAR RESONNANCE MAGNETIQUE (IRM MULTIPARAMETRIQUE)
L’IRM est une technique récente d’imagerie médicale qui permet de visualiser avec une grande précision les tissus et les organes. Elle n’entraine aucune irradiation et fait appel aux propriétés des champs magnétiques. Les indications de l’IRM s’élargissent de plus en plus. Elle peut être une aide au diagnostic ou préciser l’extension de la lésion prostatique. Il faudra attendre 6 semaines après des biopsies avant de réaliser une IRM. Elle comporte plusieurs temps Analyse morphologique :
- La pondération T2 met en évidence l’anatomie de la prostate. L’analyse systématique de la glande centrale, de la zone périphérique, de la capsule, des plexus vasculo-nerveux, des vésicules séminales, du rectum et de la vessie sera pratiquée.
- La pondération T1 permet de différencier les zones hémorragiques (après biopsies) qui sont hyper intenses en T1.
Séquence dynamique après injection de gadolinium
Cinétique de réhaussement
Analyse fonctionnelle :
- Séquence de diffusion avec recherche d’un hyper signal et calcul du gradient ADC.
- Séquence dynamique après injection de gadolinium (produit de contraste injecté pendant l’examen). Le but est d’évaluer la cinétique du rehaussement de la prostate.
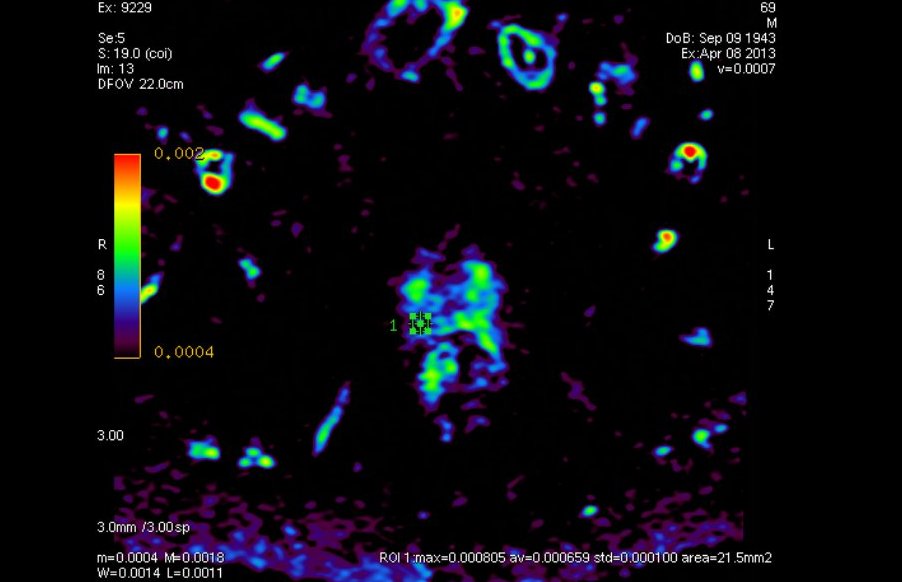
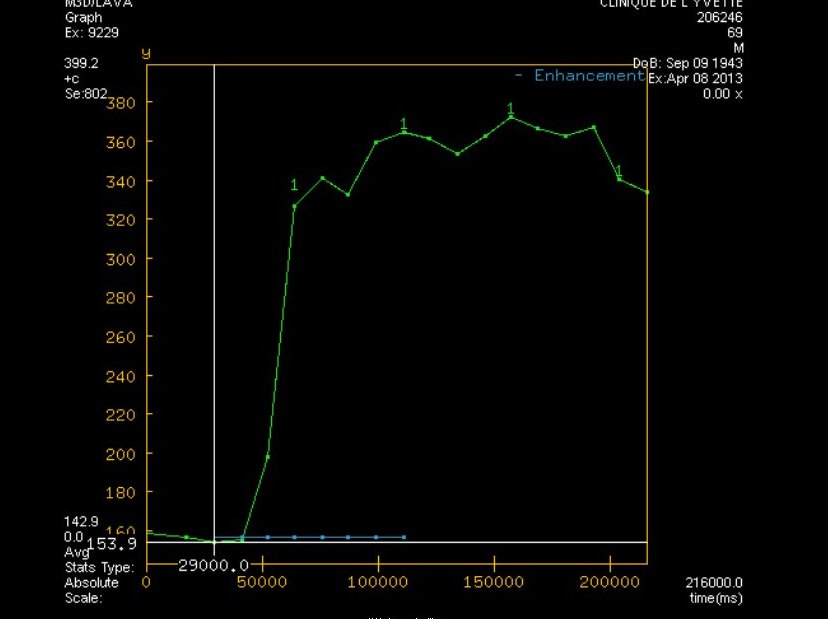
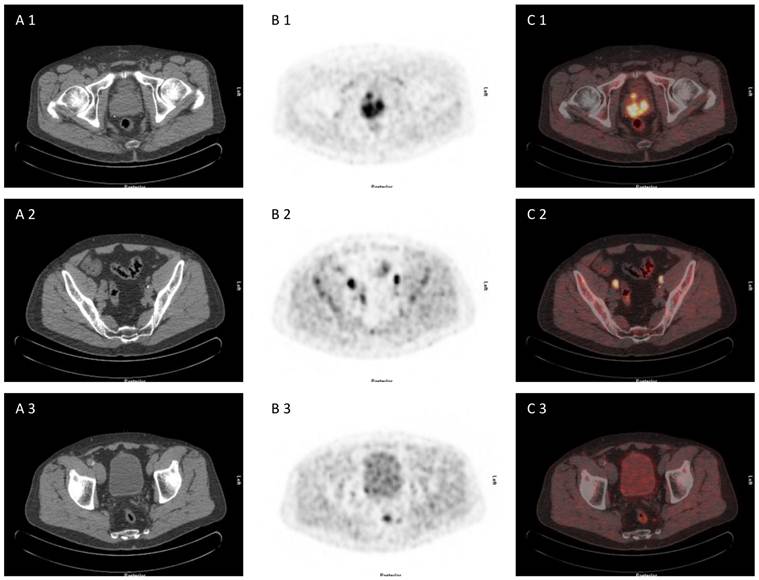
5. TEP 11C-CHOLINE OU PET SCAN À LA CHOLINE
Image PET scan d’un cancer de prostate localement avancé avec atteinte ganglionnaire.
Le pet scan combine la technique du scanner avec la tomographie d’émission de positrons. Cette nouvelle technique d’imagerie étudie le fonctionnement métabolique des tissus. Elle va rechercher une accumulation anormale d’un radio-traceur en l’occurrence la choline dans l’organisme. Sa précision globale pour définir une tumeur localisée est de 70 %. Le TEP a tendance à sous évaluer le cancer. Il a un intérêt limité chez les patients porteurs d’une lésion localisée mais il peut être utile pour la surveillance d’un patient traité en cas de réascension du PSA.
De nouveaux radiotraceurs plus sensibles apparaissent avec notamment le PSMA.
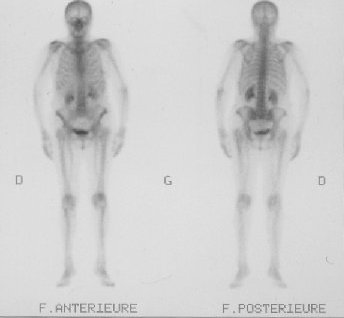
6. LA SCINTIGRAPHIE OSSEUSE
Elle étudie le squelette osseux grâce à un traceur radioactif qui se fixe sur l’os. Elle a peu d’intérêt dans les lésions localisées. Elle permet en revanche de détecter des métastases osseuses quand la maladie est évoluée. Des traumatismes osseux anciens ou de l’arthrose peuvent donner des images anormales mais bénignes.
7. Le scanner
Le scanner permet de faire un bilan d’extension du cancer de prostate mais il est de plus en plus souvent remplacé par l’IRM qui analyse la prostate localement et recherche dans le même temps une extension vers les ganglions.
8. Les biopsies prostatiques
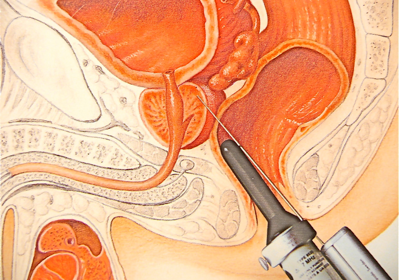
Les biopsies prostatiques se font habituellement par voie endo-rectale ou périnéale et sous contrôle échographique. Le protocole de réalisation est strict. Elles permettent de cartographier la prostate et de réaliser des biopsies dans une cible qui aurait été vue à l’IRM.
Télécharger la fiche AFU : Biopsie échoguidée de la prostate
Elles font le diagnostic de la maladie mais 10 à 30 % des cancers dits cliniquement significatifs peuvent être méconnus sur une première série de biopsies. Les biopsies prostatiques sont de plus en plus réalisées après une analyse de glande par une IRM qui peut aider à cibler certaines zones suspectes. Quand elles sont positives, elles renseignent sur l’agressivité en donnant le score de Gleason et le nombre de prélèvements atteints. Elles font partie intégrante de la surveillance des patients placés en surveillance active. La complication la plus fréquente est l’infection (moins de 2 % des cas). Si au décours des biopsies, le patient présente de la fièvre, des difficultés à uriner ou des brulures urinaires, il devra immédiatement consulter son médecin ou son urologue.
V) CLASSIFICATIONS DU CANCER DE LA PROSTATE
Le stade clinique, le grade histologique permettront avec le PSA de déterminer le traitement adapté à chaque patient.
1. STADE CLINIQUE
Il est divisé en deux catégories : Le cancer non métastatique : cliniquement localisé (confiné à la prostate) ou localement avancé (étendu en dehors de la capsule prostatique) Le cancer métastatique : étendu en dehors de la prostate. Les atteintes ganglionnaires et osseuses sont particulièrement fréquentes. Classification TNM du cancer de la prostate 2009
- T Tumeur primitive
- TX : tumeur primitive non évaluée
- T0 : tumeur primitive non retrouvée
- T1 : tumeur ni palpable au toucher rectal (TR) ni visible en imagerie
- T1a : tumeur occupant moins de 5 % du tissu réséqué
- T1b : tumeur occupant plus de 5 % du tissu réséqué
- T1c : tumeur découverte sur une biopsie prostatique en raison d’une élévation des PSA.
La classification de l’American Joint Commitee intègre le score de Gleason pour différencier le T1a du T1b : – T1a < 5 % du tissu réséqué avec un score de Gleason < 7 ou absence de grade 4 ou 5.T1b > 5 % du tissu réséqué ou un score de Gleason > 7 ou présence de grade 4 ou 5.
- T2 : tumeur limitée à la prostate
- T2a : tumeur atteignant la moitié d’un lobe ou moins
- T2b : tumeur atteignant plus de la moitié d’un lobe mais sans atteindre les deux lobes
- T2c : tumeur atteignant les deux lobes
- T3 : extension au-delà de la capsule
- T3a : extension extra-capsulaire uni- ou bilatérale
- T3b : extension aux vésicules séminales uni- ou bilatérale
- T4 : tumeur fixée ou atteignant d’autres structures que les vésicules séminales (sphincter externe, rectum, muscles releveurs de l’anus ou paroi pelvienne)
- N Ganglions régionaux
- NX : ganglions régionaux non évalués
- N0 : absence de métastase ganglionnaire régionale
- N1 : atteinte ganglionnaire régionale
- N1 mi : métastase ganglionnaire < 0,2 cm (optionnel)
Métastases à distance
- MX : métastases à distance non évaluées
- M0 : absence de métastase à distance
- M1 : métastases à distance
- M1a : atteinte des ganglions non régionaux
- M1b : atteinte osseuse
- M1c : autres sites
2. CLASSIFICATION HISTOLOGIQUE OU SCORE DE GLEASON
La classification de Gleason est fondée sur le degré de différenciation (degré d’agressivité) de la tumeur, coté du grade 1 à 5. C’est le résultat d’une étude au microscope des cellules cancéreuses, obtenues par des biopsies ou une ablation de la prostate, qui constitue un score, appelé score de Gleason. Ce score est la somme des deux grades les plus fréquemment représentés dans la tumeur analysée. Il varie habituellement de 6 à 10. Plus le score est élevé, plus la tumeur est agressive.
3. LASSIFICATION PRONOSTIQUE OU CLASSIFICATION DE D’AMICO
Des groupes à risque ont été validés pour estimer le risque de progression après prostatectomie totale, radiothérapie externe et curiethérapie interstitielle :
- Risque faible : PSA < à 10 ng/ml et score de Gleason ≤ à 6 et stade clinique T1c ou T2a.
- Risque intermédiaire : PSA entre 10 et 20 ng/ml ou score de Gleason de 7 ou stade clinique T2b.
- Risque élevé (ou haut risque): PSA > 20 ng/ml ou score de Gleason > 7 (8, 9 ou 10) ou stade clinique T2c.
Une nouvelle classification appelée ISUP est maintenant utilisée pour classer les cancers de prostate :
Le groupe ISUP 1 correspond aux cancers classés Gleason 6 (3+3). C’est le meilleur pronostic.
Le groupe ISUP 2 correspond aux cancers classés Gleason 7 (3+4)
Le groupe ISUP 3 correspond aux cancers classés Gleason 7 (4+3)
Le groupe ISUP 4 correspond aux cancers classés Gleason 8 (4+4 ou 3+5).
Le groupe ISUP 5 correspond aux cancers classés Gleaon 9 (4+5 ou 5+4) ou 10 (5+5).
VI) TRAITEMENT
1. SURVEILLANCE ACTIVE
Télécharger la fiche AFU : Surveillance active pour cancer de prostate
En 2007, aux Etats Unis, Il y a eu 240890 nouveaux cas avec seulement 33720 décès (5). Si le dépistage permet une réduction relative de la mortalité du cancer de prostate de 20 %. Le risque de surtraitement est donc important (2). Le bénéfice du traitement apparait en fait limité pour les cancers faiblement agressifs mais il semble apporter une amélioration de la survie globale pour les cancers à risque intermédiaire et de haut risque. Il parait également améliorer la survie spécifique pour le cancer à haut risque ou quand le PSA est supérieur à 10 ng/ml. La surveillance active a pour but de réduire le risque de surtraitement. Cette surveillance active ne peut être proposée qu’à des patients parfaitement sélectionnés présentant des cancers à très faible risque de progression. Il est en effet important de rappeler qu’il existe un risque significatif de progression tumoral après traitement conservateur chez certains patients présentant un cancer apparemment localisé. Différents critères ont été retenus pour proposer au patient une surveillance active. Une étude multicentrique nationale « SURACAP » (7) propose les critères suivants :
- PSA <10 g/ml
- Score de Gleason < 7
- Moins de 3 biopsies positives
- Pas de carotte envahie sur plus de 3 mm
2. PROSTATECTOMIE RADICALE :
Télécharger la fiche AFU : prostatectomie totale
A) Ce qu’il faut savoir sur la prostatectomie
- Principes chirurgicaux
- Suites post-opératoires immédiates
- Suites à distance
La prostatectomie radicale est un traitement curatif du cancer localisé de prostate. Il s’agit d’une ablation complète de toute la prostate ainsi que des vésicules séminales. Un curage ganglionnaire extensif est associé à la prostatectomie pour les tumeurs à risque intermédiaire où le risque de métastase ganglionnaire est supérieur à 5 %. Dans les autres cas, il peut être évité.
Cette intervention est le plus souvent maintenant réalisée par coelioscopie robot assistée, le chirurgien introduit des instruments robotisés par des petites incisions à travers la paroi abdominale. Cette technique lui permet d’accéder et de retirer la prostate. En l’absence de critère de gravité, la prostatectomie peut être réalisée en préservant les bandelettes neuro-vasculaires et donner ainsi au patient une chance de conserver ses érections. La préservation nerveuse nécessite une dissection proche de la glande prostatique. Si une lésion agressive est suspectée (PSA élevé, gleason ≥ 8, lésion étendue > T2c, lésion extracapsulaire à l’IRM), la préservation nerveuse doit être discutée car elle fait prendre le risque de laisser du cancer et expose à une récidive de la maladie. La prostatectomie nécessite une anesthésie générale. La durée d’hospitalisation est de quelques jours et peut même, dans certains cas, être réalisée en chirurgie ambulatoire. Une sonde vésicale est laissée en place pendant 6 – 8 jours. Le patient sort donc avec sa sonde et des soins à domicile par une infirmière. La sonde sera ensuite retirée en consultation. Le risque d’incontinence est à 1 an de 7,7% (8) Le contrôle de la continence peut être difficile après ablation de la sonde pendant une durée de quelques semaines à parfois quelques mois. Le degré d’incontinence est variable selon les patients. Même si une majorité de patient a récupéré une bonne continence à 3 mois, il est parfois nécessaire de proposer une rééducation vésico-sphinctérienne. Si les fuites urinaires persistent après un an, un traitement spécifique de l’incontinence pourra être proposé. L’impuissance qui a déjà été évoquée, est une complication habituelle qui peut être évitée quand les bandelettes neuro-vasculaires sont préservées. Les patients qui bénéficient d’une préservation nerveuse ont un risque plus important de récidive locale et doivent être parfaitement sélectionnés. Le taux d’impuissance est extrêmement variable selon les études et les auteurs. Il dépend :
- La qualité des érections avant la chirurgie.
- La qualité de la préservation des bandelettes nerveuses.
- L’âge du patient au moment de la chirurgie.
La récupération des érections peut prendre un certain temps, de quelques semaines à 2 ans. Une prise en charge post-opératoire des troubles de l’érection est indispensable. Des solutions existent : médicamenteuses, crèmes dans l’urètre, injections dans le penis ou vacuum (pompe à vide). Une prise en charge précoce peut aider à récupérer une fonction sexuelle. Le patient ne doit pas hésiter à en parler à son chirurgien.
B) Une prostatectomie pour quel cancer ?
- Les lésions T1c (augmentation isolée du PSA)
- Les cancers T2a (nodule prostatique sur moins d’un lobe)
- Les lesions T2b-T2c ou Gleason 7 ou PSA 10-20 ng/ml
Les cancers découverts à la suite d’une augmentation isolée du PSA (toucher rectal normal) sont les plus fréquents. La plupart de ces tumeurs sont significatives et ne doivent pas restées sans traitement car 30 % de ces lésions sont déjà localement évoluées sans l’examen histologique de la pièce de prostatectomie. (9) La proportion de lésions dites non significatives varie entre 11 % et 16 %. (10) La prostatectomie doit être proposée aux patients dont l’espérance de vie est supérieure à 10 ans car le risque de progression à 5 ans est de 35-55 % (11) La prostatectomie est le traitement de référence pour les patients dont l’espérance de vie est supérieure à 10 ans pour des tumeurs de risque intermédiaires. Le pronostic est excellent quand la lésion est limitée à la prostate sur l’analyse de la pièce opératoire Film Prostatectomie radicale par laparoscopie
C) Prostatectomie et traitements combinés
En cas de lésion agressive à haut risque de risque de récidive au traitement complémentaire par radiothérapie et/ou hormonothérapie peut être associé à la chirurgie. Après prostatectomie, une radiothérapie est toujours possible en cas de récidive tardive de la maladie.
3. RADIOTHERAPIE
La radiothérapie externe consiste à diriger des rayons (photons ou rayons X) produits par une source externe au niveau de la prostate pour détruire les cellules cancéreuses. Ces rayons sont émis, par un accélérateur linéaire de particules, en faisceaux ciblés sur la tumeur prostatique et parfois sur des ganglions reliés à la glande atteinte. Ce traitement est réalisé par un oncologue radiothérapeute. Les rayons provoquent des lésions de toutes les cellules irradiées qu’elles soient saines ou cancéreuses. Ce qui explique les effets secondaires de la radiothérapie. L’enjeu du traitement par radiothérapie consiste donc à concentrer son efficacité sur la prostate en limitant la toxicité sur les tissus avoisinants (vessie, rectum, canal anal). Dans ce but, de nouvelles machines se sont développées pour permettre ce que l’on appelle la radiothérapie conformationnelle. La radiothérapie conformationnelle est un type de radiothérapie externe où est utilisé un collimateur multilames. Le collimateur multilames est un dispositif spécialisé fait de barres de métal fixées à l’appareil de radiothérapie. Les barres bloquent les faisceaux de radiation dans le but de modifier la zone d’irradiation et de l’adapter à la prostate. On a recours à la tomodensitométrie (TDM) ou à la résonance magnétique (IRM) pour créer une image précise de la glande en 3D. La radiothérapie conformationnelle avec modulation d’intensité (IRMT) permet de moduler les doses dans la zone à traiter et lorsqu’elle est couplée à l’imagerie (IGRT) peut corriger l’irradiation en fonction du mouvement des organes voisins. Cette évolution de la radiothérapie permet une escalade de dose qui améliore le contrôle local de la maladie sans augmenter les effets secondaires en particulier au niveau du rectum. La dose de rayons nécessaire pour détruire une tumeur varie selon le type de cancer. La dose de tolérance des organes à risque est également variable selon les organes et selon la radiosensibilité du patient. Les doses habituellement délivrées lors d’une radiothérapie externe d’un cancer de la prostate sont de 70 à 80 Gy (1 Gy correspond à une énergie de 1 joule absorbée dans une masse de 1 kg) pour une radiothérapie exclusive. Les doses sont plus faibles en cas de radiothérapie réalisée après une prostatectomie totale. Il faut aussi jouer sur ce que l’on appelle l’étalement et le fractionnement de la dose, c’est-à-dire la durée totale du traitement et son découpage en plusieurs séances ce qui permet aux tissus de se régénérer
- Comment se déroule la radiothérapie externe :
Une phase de repérage de la zone à traiter. Elle est réalisée habituellement à l’aide d’un scanner qui permet d’obtenir une imagerie en 3D. Un calcul de la distribution de la dose (dosimétrie) Le traitement proprement dit. Les séances de radiothérapie se déroulent sur plusieurs semaines, habituellement à raison de 4 à 5 séances par semaine. Le temps d’irradiation est court de l’ordre de quelques minutes. Aucune étude randomisée n’a comparé la prostatectomie radicale et la radiothérapie conformationnelle pour le cancer localisé de la prostate. Les effets secondaires de la radiothérapie sont les diarrhées et les rectites avec selles glaireuses ou sanglantes. Les troubles urinaires sont les brulures urinaires, les mictions fréquentes, les difficultés mictionnelles ou à l’inverse l’incontinence. Les risques sexuels et l’impuissance sont possibles. En cas de récidive de la maladie, une prostatectomie de rattrapage est difficile et associée à un de taux élevé d’incontinence d’environ 50 %.
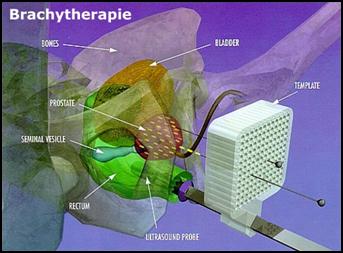
4. BRACHYTHERAPIE OU CURIETHERAPIE
La brachythérapie ou curiethérapie est une implantation par voie transpérinéale de grains d’iode (iode 125) radioactifs dans la prostate. Ces sources radioactives émettent des rayonnements qui détruisent les cellules cancéreuses. La dose de rayonnement décroit très vite au fur et à mesure que l’on s’éloigne de la source radioactive. Les effets secondaires sont donc limités sur les organes avoisinants. Le patient est pris en charge par un urologue et un oncologue radiothérapeute. Ce traitement est réservé à des patients porteurs de cancer peu agressif (stade T1C à T2a N0 M0 avec un score de gleason 6 et un PSA ≤ 10) sur une prostate de moins de 50 ml, l’absence de gêne mictionnelle significative (IPSS <12)
Technique de brachythérapie
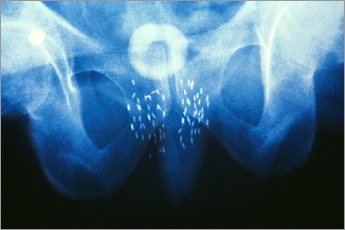
Image radiologique des grains d’iode implantés
Les complications digestives de la curiethérapie sont exceptionnelles. Les complications urinaires sont surtout marquées par des signes d’irritatifs et un risque de rétention urinaire. Le risque d’impuissance est variable selon les séries et comparable à celui des prostatectomies avec préservation des bandelettes neuro-vasculaires. Elle ne permet pas une prostatectomie de rattrapage en cas de récidive de la maladie.
5. HORMONOTHERAPIE
Le cancer de prostate est un cancer dépendant des androgènes qui stimulent la prolifération tumorale. La principale source androgénique est testiculaire et à un moindre degré les glandes surrénales. La sécrétion de testostérone est contrôlée par l’axe hypothalamo-hypophysaire. Cette testostérone pénètre dans les cellules prostatiques prostatiques où elle est transformée en dihydrotestostérone qui a un effet androgénique plus puissant. Le blocage androgénique sera proposé chez les patients métastatiques ou en cas de traitement combiné pour les maladies localisées ou localement avancées. Les effets secondaires les plus fréquents sont les bouffées de chaleur, l’impuissance, la perte de libido, la prise de poids et les complications cardiovasculaires. La castration peut être chimique ou chirurgicale. a) Pulpectomie ou castration chirugicale Elle permet une diminution immédiate de la testostérone, elle est peu couteuse mais irréversible. Elle n’est quasiment plus réalisée b) Les agonistes de la LH-RH (buséréline, goséréline, leuproréline, triptoréline) Une administration prolongée de LHRH avec perte de la pulsatilité physiologique de LHRH qui provoque une désensibilisation hypophysaire et un effondrement consécutif de la sécrétion de LH et de FSH réalisant une castration chimique. c) les antagonistes de la LHRH (dégarélix) Ils provoquent une inhibition immédiate du mécanisme de production. d) Les antiandrogènes non stéroidiens (nilutamide, flutamide et bicalutamide) Ils entrainent une inhibition compétitive des androgènes en se liant aux récepteurs aux androgènes dans le noyau de la cellule prostatique. Ils peuvent être envisagés dans plusieurs circonstances : Lors de l’initiation de la castration par analogue pour éviter l’effet « flare-up ». En cas de progression biologique sous analogue de la LHRH D’emblée en association aux analogues, dans le cadre d’un blocage androgénique complet (association analogue LHRH et anti-androgène) dont le bénéfice reste discuté.
Plus récemment sont apparues des hormonothérapies de deuxième génération permettant une amélioration de la survie globale et des symptômes au prix d’effets secondaires raisonnables
VII) SURVEILLANCE
1. Surveillance après traitement curatif
Après prostatectomie radicale, radiothérapie externe ou curiethérapie, une surveillance régulière est recommandée. Le suivi sera fait par dosage du PSA
2. Surveillance du traitement hormonal
Le PSA est encore le marqueur de choix pour la surveillance d’un patient sous traitement hormonal. Il permet d’évaluer l’étendue de la maladie métastatique puis la réponse au traitement. Il identifiera un éventuel échappement thérapeutique. La testostéronémie. Une testostéronémie au-dessus du seuil de castration (20 ng/dl) est un signe d’inefficacité du traitement qui doit faire envisager une modification de l’hormonothérapie. Les patients devront également bénéficier d’un suivi osseux métabolique et cardiovasculaire. Le rythme de la surveillance est habituellement de 6 mois sauf à l’initiation du traitement et en cas de résistance au traitement. Il est évidement adapté à chaque patient.
Références
- Mortality results from a randomized prostate-cancer screening trial. Andriole GL, Crawford ED, Grubb RL 3rd, Buys SS, Chia D, Church TR, Fouad MN, Gelmann EP, Kvale PA, Reding DJ, Weissfeld JL, Yokochi LA, O’Brien B, Clapp JD, Rathmell JM, Riley TL, Hayes RB, Kramer BS, Izmirlian G, Miller AB, Pinsky PF, Prorok PC, Gohagan JK, Berg CD; PLCO Project Team. N Engl J Med. 2009 Mar 26;360(13):1310-9. doi: 10.1056/NEJMoa0810696. Epub 2009 Mar 18. Erratum in: N Engl J Med. 2009 Apr 23;360(17):1797.
- Screening and prostate-cancer mortality in a randomized European study. Schröder FH, Hugosson J, Roobol MJ, Tammela TL, Ciatto S, Nelen V, Kwiatkowski M, Lujan M, Lilja H, Zappa M, Denis LJ, Recker F, Berenguer A, Määttänen L, Bangma CH, Aus G, Villers A, Rebillard X, van der Kwast T, Blijenberg BG, Moss SM, de Koning HJ, Auvinen A; ERSPC Investigators. N Engl J Med. 2009 Mar 26;360(13):1320-8. doi: 10.1056/NEJMoa0810084. Epub 2009 Mar 18.
- The role of the digital rectal examination in subsequent screening visits in the European randomized study of screening for prostate cancer (ERSPC), Rotterdam. Gosselaar C, Roobol MJ, Roemeling S, Schröder FH. Eur Urol. 2008 Sep;54(3):581-8. doi: 10.1016/j.eururo.2008.03.104. Epub 2008 Apr 8.
- Use of the percentage of free prostate-specific antigen to enhance differentiation of prostate cancer from benign prostatic disease: a prospective multicenter clinical trial. Catalona WJ, Partin AW, Slawin KM, Brawer MK, Flanigan RC, Patel A, Richie JP, deKernion JB, Walsh PC, Scardino PT, Lange PH, Subong EN, Parson RE, Gasior GH, Loveland KG, Southwick PC. JAMA. 1998 May 20;279(19):1542-7.
- Cancer: fact and figures 2011. America cancer society. 2011 (web base: http://www.cancer.org/ Research/CancerFactsFigures/CancerFactsFigures/cancer-facts-figures-2011)
- Wilt TJ. The VA/NCI/AHRQ CSP#407: Prostate Cancer Intervention Versus Observation Trial (PIVOT): main results from a randomized trial comparing radical prostatectomy to watchful waiting in men with clinically localized prostate cancer. Plenary presentation at: American Urological Association Annual
- Mottet N, Irani J. Active surveillance in prostate cancer: the French protocol. Prog Urol FMC 2008:F12–F16.
- National patterns of prostate cancer treatment by radical prostatectomy: results of a survey by the American College of Surgeons Commission on Cancer. Murphy GP, Mettlin C, Menck H, Winchester DP, Davidson AM. J Urol. 1994 Nov;152(5 Pt 2):1817-9.
- Impalpable invisible stage T1c prostate cancer: characteristics and clinical relevance in 100 radical prostatectomy specimens–a different view. Elgamal AA, Van Poppel HP, Van de Voorde WM, Van Dorpe JA, Oyen RH, Baert LV. J Urol. 1997 Jan;157(1):244-50.
- PSA-detected (clinical stage T1c or B0) prostate cancer. Pathologically significant tumors. Oesterling JE, Suman VJ, Zincke H, Bostwick DG. Urol Clin North Am. 1993 Nov;20(4):687-93.
- The significance of low-grade prostate cancer on needle biopsy. A radical prostatectomy study of tumor grade, volume, and stage of the biopsied and multifocal tumor. Epstein JI, Steinberg GD. Cancer. 1990 Nov 1;66(9):1927-32